·
O que caracteriza a matéria:
- Para a ciência é tudo aquilo que apresenta massa e ocupa
lugar no espaço.
- As substâncias formam vários materiais.
- A Química é uma ciência que estuda a matéria, suas
propriedades e transformações.
- A constituição das substâncias e o modelo de partículas:
-> Percebeu-se que as substâncias eram proporções de
matéria com composição fixa, sugerindo que as substâncias eram constituídas por pequenas unidades, sendo denominadas partículas, que se combinavam sempre
da mesma forma.
- Um modelo científico sempre apresenta limitações.
- O modelo das partículas é usado para entender a composição
da matéria e explicar várias propriedades observadas nas substâncias.
·
Massa:
- É uma grandeza
física relacionada à inércia de um corpo.
- Unidade (SI): kg.
·
Volume:
- É o espaço ocupado por um corpo.
- Unidade de medida ( SI) : metro cúbico).
- Variação do volume e o modelo de partículas:
-> quanto maior a pressão, mais próximas ficam as
partículas, e assim, menor o volume.
-> quanto maior a temperatura, maior o volume.
·
Densidade:
d = massa / volume
OBS: Quando a pressão de um sistema diminui, as partículas
passam a ocupar um espaço maior, portanto, o volume aumenta, sem a variação da
massa, a densidade fica menor.
·
Solubilidade:
- Solvente: substância presente em maior quantidade.
- Soluto: substância em menor quantidade.
- Solução: mistura homogênea.
- Limite de solubilidade:
-> Insaturada: abaixo do limite de solubilidade.
-> Saturada: no limite de solubilidade.
- A solubilidade e o
modelo de partículas: as partículas se movimentam aleatoriamente, de modo
gradativo nos espaços entre elas, até se transformar em uma distribuição
homogênea.
·
Condutibilidade elétrica:
- A escolha dos materiais é feita de acordo com as suas
propriedades.
- Varia para os diferentes materiais.
·
Condutibilidade térmica:
- Quando tocamos diferentes materiais à mesma temperatura,
pode-se senti-los frios ou quentes.
- A condutibilidade térmica e o modelo de partículas:
- Fluxo de energia = calor.
- O calor é transferido até atingir o equilíbrio térmico.
·
Propriedades organolépticas:
- Odor.
- Cor.
- Textura.
- Sabor.
·
Organização interna da matéria:
- As fases possuem:
-> características físicas uniformes.
-> composição química homogênea.
- Interações entre partículas:


- Mudanças de fases:
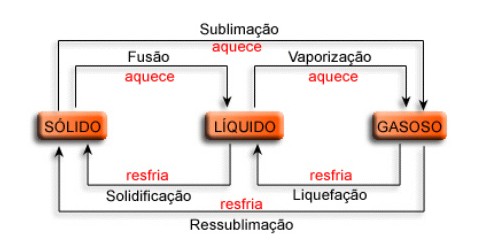
-> Temperatura de fusão: sólido para líquido.
-> Temperatura de ebulição: líquido para gasoso.
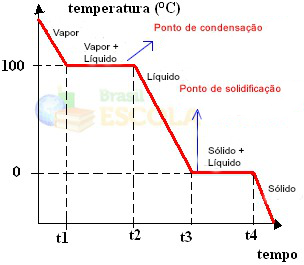
- Transformações químicas:
- Alteram a composição do material original.
- Indícios de transformações químicas:
- Evidências macroscópicas: através dessas evidências as alterações são perceptíveis.
-> Calor e reações químicas:
Reações exotérmicas: o calor é transferido do sistema reacional para a vizinhança.
Reações endotérmicas: transferência de calor da vizinhança para o sistema.
- Como impedir uma reação química:
Nenhum comentário:
Postar um comentário